Ensayo Aptima™ HCV Quant Dx
Diagnóstico de la infección activa y monitorización de la carga viral del virus de la hepatitis C (VHC).1

Alta sensibilidad de detección
El ensayo proporciona resultados precisos y exactos en todos los principales genotipos. Posee una excelente sensibilidad y una alta precisión, incluso con muestras de baja viremia.1 El procesamiento del ensayo Aptima HCV Quant Dx en el sistema Panther® combina un alto rendimiento analítico con una excelente automatización, desde la muestra al resultado con un único equipo integrado.1
Flujo de trabajo eficiente y procesamiento flexible
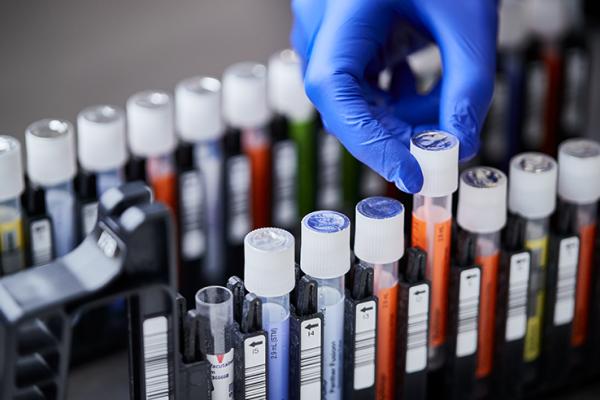
Validado para uso de tubos EDTA para diversas muestras, tubos para preparación de plasma ACD y EDTA.1Posibilidad de procesar varias pruebas a partir de una única muestra. Sin preparación manual de muestras y con carga de tubos primarios para mantener la identificación positiva de las muestras.
Acceso aleatorio y reducción del tiempo de procesamiento
El procesamiento por lotes ha pasado a la historia. Ahora es posible procesar muestras con diferentes peticiones de análisis a medida que llegan al laboratorio. Reducción del tiempo de procesamiento, con los primeros resultados al cabo de tan solo 2 horas y 41 minutos. Priorización de resultados STAT.2
Análisis y factor de dilución automáticos
Análisis de control de calidad automático mediante gráficos de Levey-Jennings para el seguimiento y análisis de tendencias de los controles. Opción de bajo volumen de muestra (240 μl) y factor de dilución automático, lo que elimina la necesidad de efectuar cálculos manuales.1,2
Simplificar y escalar el futuro del diagnóstico
El ensayo Aptima HCV Quant Dx forma parte de las soluciones moleculares escalables de Hologic, una gama de productos que combinan un amplio y competitivo menú de ensayos con procesos de automatización de alto rendimiento. Está diseñado para permitirle una mayor flexibilidad en la realización de las pruebas, desde la obtención de resultados para un solo paciente hasta un cribado a nivel poblacional.

Excelente sensibilidad y alta precisión
Incluso con muestras de baja viremia.1
4,3 UI/ml
Plasma
Límite de detección (LD)
3,9 UI/ml
Suero
Límite de detección (LD)
10 UI/ml*
Límite inferior de cuantificación (LIC)
10 a 100 millones de UI/ml
Rango lineal
Ponemos el listón más alto1 en las pruebas del VHC
- Uso previsto: Diagnóstico de la infección activa por VHC y monitorización de la carga viral
- Tecnología: amplificación mediada por transcripción (TMA) en tiempo real
- Región diana: región altamente conservada del ARN del VHC (5' UTR)
- Genotipos: 1-6
- Tipos de muestra: Plasma y suero

Mejora de los tratamientos
El VHC es un patógeno de transmisión hemática que representa una carga para la salud pública mundial, con hasta 170 millones de personas infectadas en todo el mundo y 350 000 muertes anuales.3,4 La cuantificación del ARN del VHC (carga viral) ha desempeñado un papel fundamental a la hora de definir tratamientos del VHC satisfactorios y monitorizarlos de forma adecuada. La respuesta viral mantenida (RVM) (es decir, la no detección de ARN del VHC después de un tratamiento satisfactorio) es un marcador esencial de la remisión de la infección por VHC.5,6 En la era de los antivirales de acción directa (AAD), los niveles de carga viral del VHC se determinan antes del tratamiento (para definir la carga viral basal), durante el tratamiento (para observar la respuesta del paciente) y después del tratamiento (para evaluar la RVM o la recaída).4-6
Datos científicos. Perspectiva. Colaboración.
Nuestro portal educativo mejora la atención al paciente a través de la excelencia en la educación, la comunicación de evidencia clínica y científica, y las alianzas con la comunidad de atención médica.
Perspectivas
* El LIC se estableció en todos los genotipos (consulte el prospecto, apartado «Determinación del límite inferior de cuantificación (LIC) en todos los genotipos del VHC»). Estos datos de genotipo determinan un LIC total de 10 UI/ml para el ensayo.
Ensayo Aptima HCV Quant Dx [prospecto]. AW-13249-001. Rev. 005 San Diego, CA; Hologic, Inc., 2019.
Manual de usuario del sistema Panther/Panther Fusion. AW-26055-001. Rev. 001
Averhoff FM, Glass N y Holtzman D. Global Burden of Hepatitis C: Considerations for Healthcare Providers in the United States. Clinical Infectious Diseases 2012; 55 (S1): S10-15.
Current and Future Disease Progression of the Chronic HCV Population in the United States (2013). PLOS ONE, volumen 8: número 5; 1-10.
Rutter, K, Hofer H, Beinhardt, S et al., Durability of SVR in chronic hepatitis C patients treated with peginterferon-α2a/ribavirin in combination with a direct acting antiviral. Aliment Pharmacol Ther. 2013 Jul; 38(2):118-23.
Kohli A, Shaffer A, Sherman A, et al. Treatment of Hepatitis C, A Systemic Review (2014). JAMA. 2014 Aug 13; 312(6): 631-640.
Documentos
Fichas de seguridad
Prospectos
Productos relacionados
1434
2797
Hologic BV, Da Vincilaan 5, 1930 Zaventem, Belgium.
Número del organismo notificado cuando proceda